Mi ESK
Minden speciális sejtek a felnőtt szervezet származnak őssejteket. Őssejtek - a "tartalék", "NC" az információ (embriogenezis). Ezt az információt nem lehet csökkenteni a fejlesztési gének, mint a fejlesztés minden fázisában nem lett beprogramozva, hogy automatikusan és kapcsolódó rendelkezésére a jelek és epigenetikai információkat. ESC - egy olyan program, és a processzor információt egyszerre. Program fejlesztése nagyban függ a környezetet. Időben frissítés repertura egészséges sejtek elengedhetetlen feltétele az egészségügyi és a hosszú élet egy többsejtű szervezetben. Minden szervet felnőtt emberek és emlősök is „emlékek” az embrionális szövetből mikrovkrapleny őssejteket. Őssejtek - a szervezet sürgető makroreparatsii masszív szövetkárosodást. Ugyanakkor őssejtek - olyan eszköz, frissítés, módosítsa elavult „beteg” sejtek, köztük elleni védelem korai öregedést. ESC megszabadulni beteg sejtek nem használ gyógyszerek, valamint időbeni változása sejteket.
A fő gondolata a molekuláris orvostudomány -, hogy megtalálják a gyógymódot, hogy meggyógyítsa a betegeket kletkok - úgy néz ki, vonzó, de praktikus. Ha az érintett szerv blokkolt sejt önmegújító, felhalmozódása számos abnormális sejtek különböző fenotípus. Ebben az esetben lenne szükség egy millió „mágikus golyó” normalizálására millió különböző beteg sejtekre. Gyakran funkcionális parenchima szervek helyébe eredetű mezenchimális (fibrózis, ateroszklerotikus plakk, gliózist stb). Csak az időben a visszanyerési tényezők parenchyma védheti szervek széles körű elterjedése a kötőszövet.

1-1 ábra Laboratóriumi módon megszerzésének származékok az emberi szövetet totipotens ESC és ACC
nem „program” a kezelés a genom szomatikus sejtek. Genomics rendellenes sejtek apoptózis használ több lehetőség autoeliminatsii kóros sejteket. Másrészt transzplantáció SC felgyorsítja sejt önmaga megújítására a szervekben, beleértve a rendellenes sejtek.
Az ESC jellemzi két változata programozott viselkedés kultúra. 1) éretlen hosszú PGC proliferálnak jelenlétében tápréteg sejtek és növekedési faktorok. 2) után a működési idő differenciálatlan sejtek tömegének, sejt ramnozhenie megállt megváltoztatásával tenyésztési körülmények között. sejtdifferenciálódást kezdődik (előnyösen egy típusú specializált sejtek). (1-1 ábra)
Ezért ESC vonalak alaposan tesztelt a rákkeltő esetében közvetlen állat. Transzplantációs hESCs az agyban soha nem kísérte a megjelenése szívizomsejtek, izomsejtek, vagy a bőrön. Másfelől, a szívátültetést ESC megakadályozta neuronok és kiválasztó sejtek a bél. Helyi differenciálódását hESCs insitu. Általában által vezérelt „jeleket” mikrokörnyezet. Totipotenciája emberi GSZT ellenőrzött nyilvánvaló okokból csak állatokon. Korlátozott klinikai megfigyelések is megerősítette, hogy nincs rendellenességek differenciálódásának őssejtek a graft.
A növekedés a hESCs tenyészetben klón. Ellentétben a hagyományos exponenciális szaporodása tenyészetben, a klón nem nő és a saját megújítani. Csak klón megtartott mikrokörnyezet, amely lehetővé teszi az őssejtek megőrzése szokatlanul magas genetikai lehetségesség. Ez különösen a sejt genomika mentve, és reprodukálni csak egy sűrű területen. Valamennyi tenyészetet hESCs van mentén változik a frakció sejtek a szuszpenzió egységek (szektorok). Egyetlen sejteket, így a klón elkerülhetetlenül differenciált. Csak egységek alkotják a teljes terület pluripotens sejtek, a maradék sejteket szakosodott hatása alatt a mikrokörnyezet. A legtöbb új fenotípus történik a periférián a klónok. Mindegyik klón sejtek differenciálódnak egyidejűleg különböző fenotípusok, megerősítve a mikrokörnyezet (mozaik utasítás jelek is igen változatos, még ugyanabban a klón).
A fejlettebb sejtek nemcsak versengett őssejtek, éretlen korlátozására táplálkozási tényezők, hanem a közegbe szekretált faktorok blokkoló pluripotencia genomjába éretlen sejtek. A tenyésztést őssejtek mindig elindul egy szelektív táptalajon, ahol 99% a sejtek meghalt fejlett, és egy kis része a túlélő őssejtek kezdett szaporodni.

Ábra 1-2. Főbb jellemzők ESK
származási hely: epiblast sejtek szex progenitor sejtek, melyen a donor sejtmag a citoplazma a petesejt
stabil proliferáció nélkül a genetikai módosítás és onko-immortalizáció
Ábra 1-3B Klón ESC, hogy a vonat migráló sejtek (fáziskontraszt-mikroszkóppal)
ESC transzplantációra szedercsíra, ahol mitoses leállítjuk tsitokalazinom, megszületéséhez vezetett az embriók, a szerveket begyűjtöttük kizárólag a donor sejteket. Nondeveloping morula fontos szerepet játszott térbeli mátrix, útmutató-D-3-kölcsönhatás hESCs. Új embriót a fejlődő és a donor ESC alapján tetraploid blasztomerek amelyek közvetlenül nem vesz részt a fejlesztés.
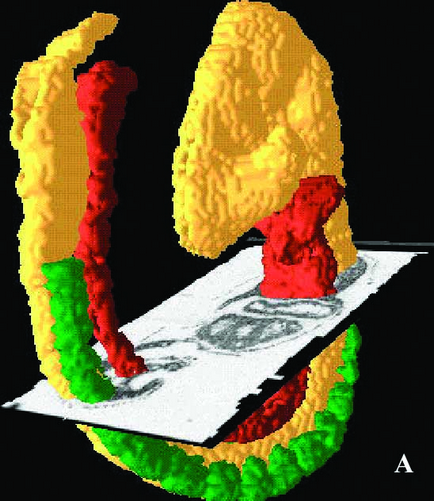

1-4 ábra Klonális szervezet totipotens embrió szövetből a szakaszában organogenezis
A számítógépes 3D-modellje az embrió
B-sejt klón ideiglenes lekötetlen alatt pásztázó elektronmikroszkópos
B klón ideiglenes nem kötött sejteket
D, D- sejt-sejt kölcsönhatások klón
Transzplantációs normál PGC egy embrió Crypto - / - hagyjuk, hogy egy elsődleges kiméra csík - egy második kritikus ideiglenesen pluripotens szövetet. Egy kialakítási lépését a tengelyek a epiblast és áttelepítése módon jelöltünk expressziója a következő gének: HES-sel 1, Lim-1, HNF3, Otx-2. Ezek a gének szükségesek megindítását embrió szegmentáció. Bármely knock-out mutáció ezen gének részlegesen vagy teljesen ellensúlyozta a átadása normál hESCs a epiblast. Számos normál totipotens sejtek az embrió elég ahhoz, hogy korlátozza szakaszában organogenesis amely ideiglenesen működik transzkriptáz (Crypto típus). Korai fejlesztés a mozaik gének szerepelnek csak a epiblast, nem egyszer minden sejtben. Ez új távlatokat nyit a magzati sejt rekonstrukciója örökletes és teratogenesis. Megbízható vizualizációs epiblast sejtek csak akkor lehetséges, segítségével színes fehérjék, alá helyezzük egy promoter a korai gének (például, Crypto-gén).
ESC eredetű szomatikus sejtmag transzfer, megalapozta az utat
Kiültetés őssejtek, a kísérletvezető megismétli a „vak játék,” evolúció a agysejtek, megnyitva az utat őssejtek részt vesz a gyülekezési és válogatása CNS hálózatokat. Ha az evolúció vak vizsgálatok ESC lehetőségeket a szerelvény szervek, a kísérletvezető keres ötleteket és megerősítését, hogyan őssejteket fel lehet használni a gyógyászatban betegségek kezelésére. Hangsúlyozni kell, hogy a kísérletek transzplantáció emberi GSZT mindig korlátozott állatkísérletek. Nem ismerik az állatoknál nem lehet elegendő és teljes magyarázatot a platform tesztelésére az emberi GSZT. Csak egy orvos, nem a kísérletvezető határozza meg az új kritériumok és kockázati mérték, ami lehetővé teszi, hogy kezdeni klinikai vizsgálatok őssejtek új módon segít a beteg emberek, maradék, kezelés nélkül annak érdekében, hogy mentse, vagy meghosszabbítja az életüket. Szigorú szabályok és kritériumok lefordítani tudás predklinki tetején a klinikai vizsgálat, látszólag nem létezik összetettsége miatt, és nem megismételhető sok esetben az ágy mellett, ahol elkezdte eljáró tapasztalat és szakértelem az orvos. Alapvető vizsgálatok hESCs csak egy része annak tudatában, hogy az orvos használ, hogy a döntéseket az új helyzetekben.